2022-02-18 17:00
细胞药物的开发正在以快速的步伐稳健推进着,这是大势所趋。从早期对干细胞疗法的质疑,到现在似乎又重新变成一个充满活力的新兴行业。国家和地方的一系列政策和奖励也在为细胞技术的发展提供了强大的支持与保障。
让我们一起看看,近期干细胞药物临床试验注册申报方面的亮点。
临床试验默许:人羊膜上皮干细胞注射液
2022年2月15日,上海赛傲生物技术有限公司申报的“人羊膜上皮干细胞注射液”(受理号:CXSL2101456)获得国家药审中心(CDE)的临床试验默示许可。
受理号为:CXSL2101456
药品名称:人羊膜上皮干细胞注射液
适应症:移植物抗宿主病
申报企业:上海赛傲生物技术有限公司
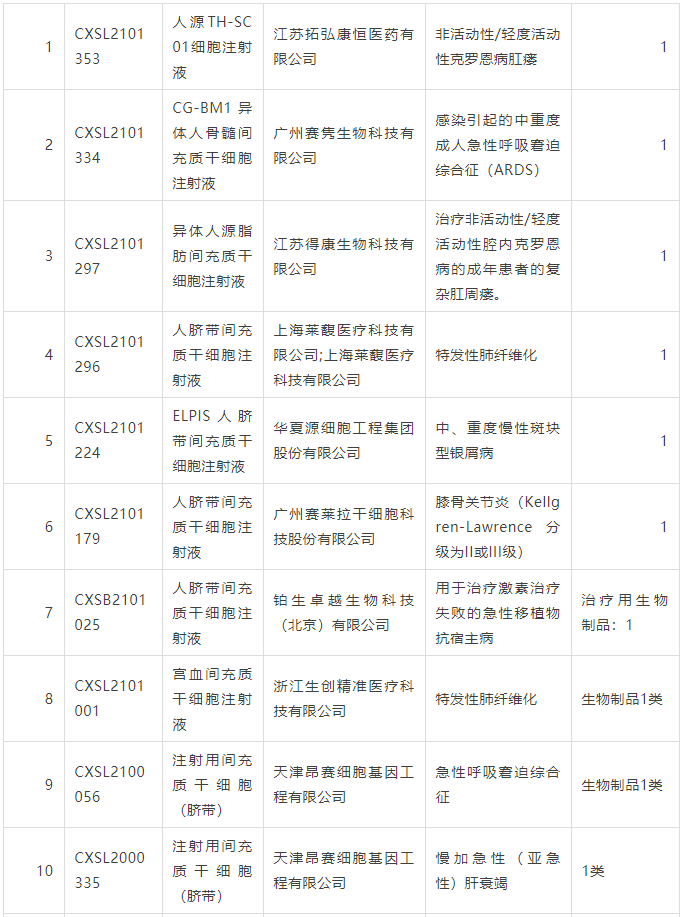
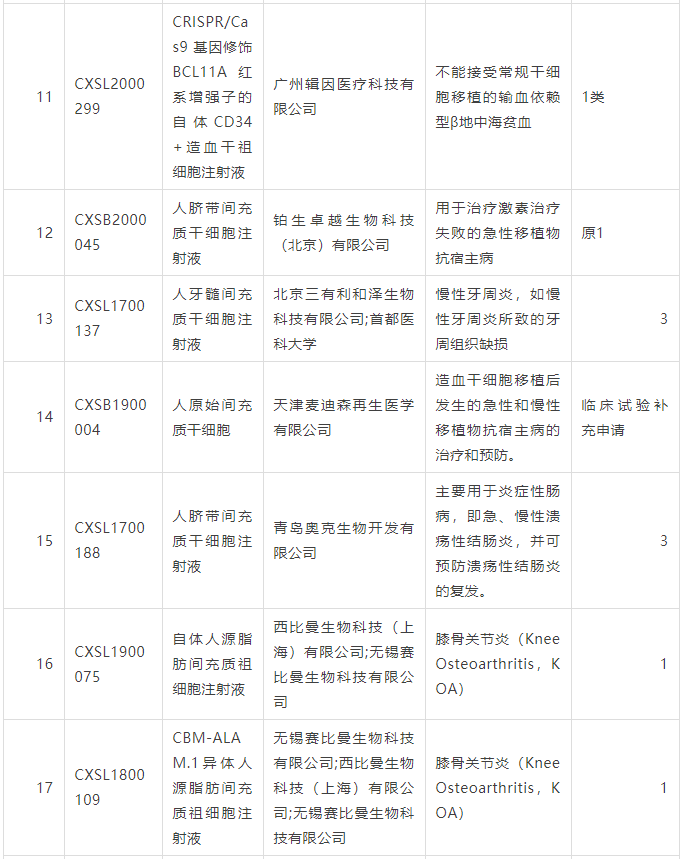
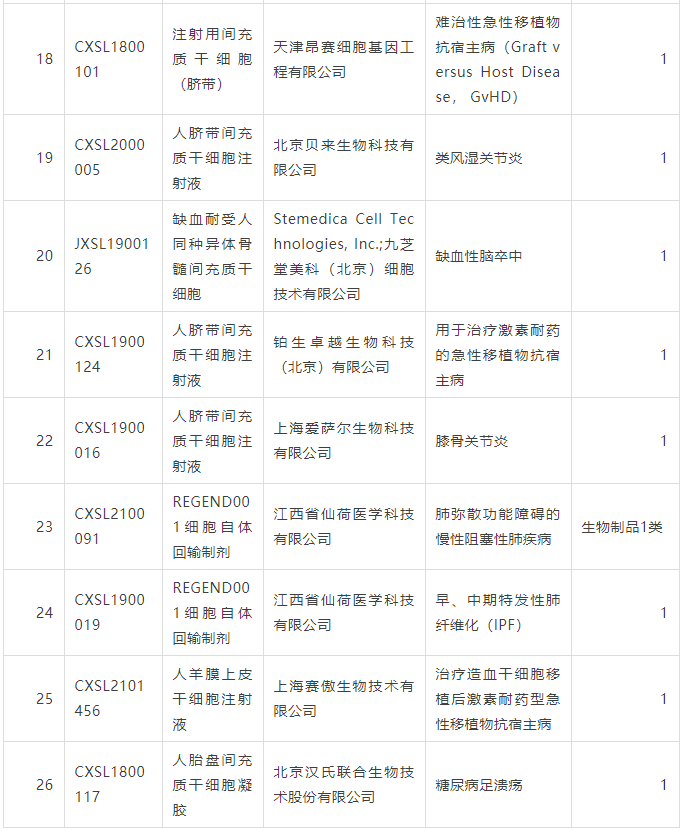
截止至2022年2月15日,我国已经通过IND的干细胞药物,已达26个。
主要细胞种类是不同来源的间充质干细胞,个别是造血干细胞。
涉及病种包括膝关节炎、溃疡性结肠炎(克罗恩病)、GVHD、特发性肺纤维化、银屑病、ARDS、肝衰、地中海贫血、牙周炎、脑卒中、糖尿病足等。下面是所有通过国家药监局药品审评中心临床试验默示许可的干细胞药物列表: